
เคมี - การจัดเรียงอิเล็กตรอน

จำนวนอิเล็กตรอนที่มีได้มากที่สุดในแต่ละระดับพลังงาน = 2n2
เมื่อ n แทนลำดับพลังงาน (มีค่า = 1, 2, 3, …..ตามลำดับ)
ระดับพลังงาน n = 1 มีจำนวนอิเล็กตรอนได้มากที่สุด = 2 ตัว
ระดับพลังงาน n = 2 มีจำนวนอิเล็กตรอนได้มากที่สุด = 8 ตัว
ระดับพลังงาน n = 3 มีจำนวนอิเล็กตรอนได้มากที่สุด = 18 ตัว
ระดับพลังงาน n = 4 มีจำนวนอิเล็กตรอนได้มากที่สุด = 32 ตัว
แต่สูตรการหาจำนวนอิเล็กตรอนดังกล่าวใช้ใด้กับระดับพลังงาน n = 1 ถึง 4 เท่านั้น เพราะในระดับพลังงานต่อ ๆ ไปจะมีอิเล็กตรอนไม่เกิน 32 นอกจากนั้นการศึกษาค่าพลังงานไอออไนเซชัน โดยเรียก อิเล็กตรอนวงนอกสุดว่า เวเลนซ์อิเล็กตรอน
การจัดเรียงอิเล็กตรอน แบบใช้หลัก 2 8 18 32 (สำหรับธาตุหมู่ 1A ถึงหมู่ 8A)
- ให้จัดอิเล็กตรอนทั้งหมด โดยเรียงจำนวนตามขั้นบันไดขึ้นด้านบน
- เมื่อไม่สามารถจัดอิเล็กตรอนขั้นถัดไป ให้จัดอิเล็กตรอนในบันไดขั้นเดิมได้ 1 ครั้งหรือขั้นที่ลดลงมา โดยอิเล็กตรอนหลักสุดท้ายจะต้องมีจำนวนอิเล็กตรอนไม่เกิน 8 ตัว เสมอ
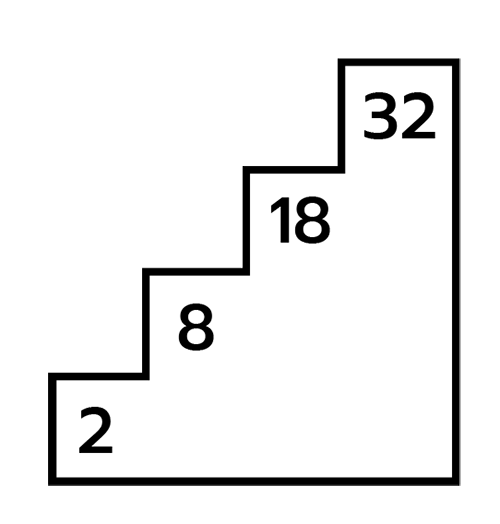
- เลขหมู่ จะตรงกับเลขหลักสุดท้ายของการจัดเรียงอิเล็กตรอน ดังนั้น ธาตุที่อยู่หมู่เดียวกันจะมีเวเลนซ์อิเล็กตรอนเท่ากัน
- จำนวนหลักของระดับพลังงาน จะตรงกับเลขของคาบ ดังนั้น ธาตุในคาบเดียวกันจะมีจำนวนระดับพลังงานเท่ากัน
การจัดเรียงอิเล็กตรอนในระดับพลังงานย่อยต้องอาศัยหลักการต่าง ๆ ดังนี้
1. หลักกีดกันของเพาลี ในการบรรจุอิเล็กตรอนในออร์บิทัลซึ่งจะเขียนแทนด้วยสัญลักษณ์ ส่วนอิเล็กตรอนจะใช้ลูกศร เช่น ↑ สำหรับสปินขึ้น และ ↓ สำหรับสปินลง ถ้าออร์บิทัลมีอิเล็กตรอนอยู่เต็มจะเขียนแทนด้วยรูปภาพ ↥⤓ เรียกอิเล็กตรอนทั้งสองว่า อิเล็กตรอนคู่ ถ้ามีอิเล็กตรอนเพียงครึ่งหนึ่ง นิยมเขียนเป็นสปินขึ้น ↥ และเรียกว่า อิเล็กตรอนเดี่ยว
2. กฎของฮุนด์กล่าวว่า “ลักษณะที่ทำให้มีอิเล็กตรอนเดี่ยวมากที่สุดเท่าที่จะมากได้” ถ้าทุกๆ ออร์บิทัลในระดับพลังงานเดียวกันนั้น มีอิเล็กตรอนอยู่เต็ม (2 อิเล็กตรอนต่อ 1 ออร์บิทัล) เรียกว่าเป็น การบรรจุเต็ม (full-filled configuration) แต่ถ้ามีอิเล็กตรอนอยู่เพียงครึ่งเดียว (1 อิเล็กตรอนต่อ 1 ออร์บิทัล) เหมือนกันหมด เราเรียกว่าเป็น การบรรจุครึ่ง (half-filled configuration)
3. หลักอาฟบาว กล่าวว่า การบรรจุอิเล็กตรอนลงในแต่ละออร์บิทัลจะต้องบรรจุลงในออร์บิทัลที่มีพลังงานต่ำสุดก่อน แล้วจึงบรรจุอิเล็กตรอนลงในออร์บิทัลถัดไปที่มีพลังงานสูงขึ้นตามระดับพลังงานต่ำไปสูง ซึ่งไปตามแผนผังดังนี้
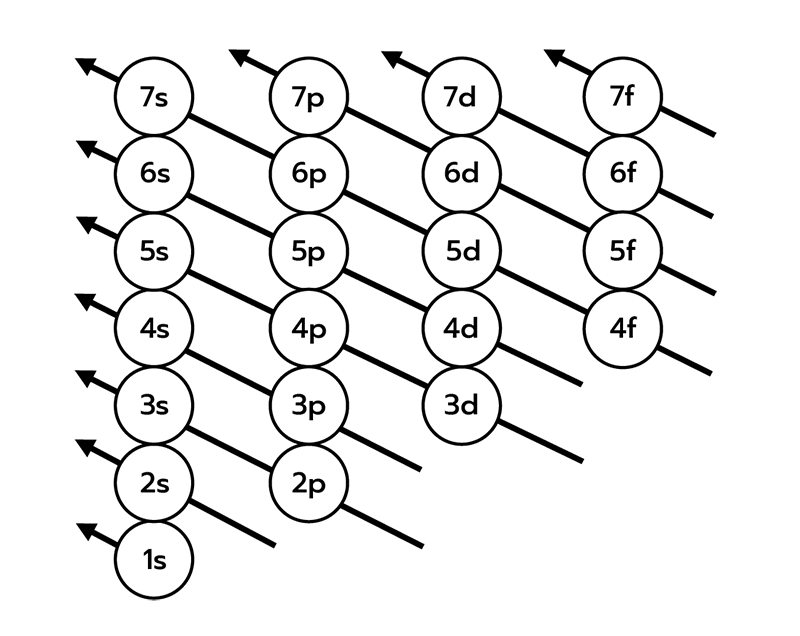

มีบทต่อไป ->

ดร.ณัฏฐพล อิสรเสรีรักษ์
● ปริญญาตรี โท เอก คณะวิทยาศาสตร์ จุฬาฯ
บัณฑิตศึกษาปริญญาโทที่มีผลการเรียนดีเด่น (รางวัล ดร.แถบ นีละนิธิ)
● อาจารย์พิเศษ วิชาเคมี ห้องเรียนพิเศษ gifted โรงเรียนมัธยม
● วิทยากรรับเชิญ เตรียมสอบ O-NET วิชาวิทยาศาสตร์ ม.ต้น ม.ปลาย
● วิทยากรรับเชิญเตรียมสอบ PAT2 และ วิชาสามัญ (เคมี)

